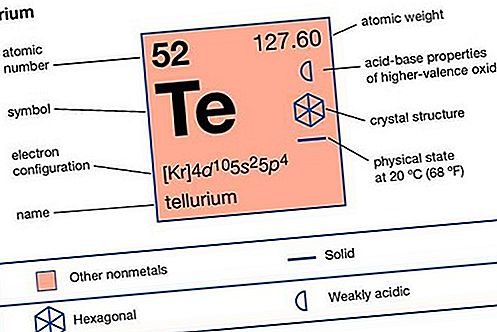
Tellure (Te), élément chimique semi-métallique du groupe oxygène (Groupe 16 [VIa] du tableau périodique), étroitement associé à l'élément sélénium dans ses propriétés chimiques et physiques. Le tellure est un élément blanc argenté avec des propriétés intermédiaires entre celles des métaux et des non-métaux; il représente environ une partie par milliard de la croûte terrestre. Comme le sélénium, il est moins souvent trouvé non combiné que sous forme de composés de métaux tels que le cuivre, le plomb, l'argent ou l'or et est obtenu principalement comme sous-produit du raffinage du cuivre ou du plomb. Aucune utilisation importante du tellure n'a été trouvée.

élément du groupe oxygène: présence naturelle et utilisations
Le tellure est un élément blanc argenté (symbole Te) avec des propriétés intermédiaires entre celles des métaux et des non-métaux; il
.Propriétés des éléments
| numéro atomique | 52 |
|---|---|
| poids atomique | 127,60 |
| masses d'isotopes stables | 120, 122, 123, 124, 125, 126, 128, 130 |
| point de fusion | 449,8 ° C (841,6 ° F) |
| point d'ébullition | 989,9 ° C (1813,8 ° F) |
| états d'oxydation | −2, +2, +4, +6 |
| configuration électronique | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 4 |
Histoire
L'élément tellure a été isolé avant d'être connu comme étant une espèce élémentaire. Vers 1782, Franz Joseph Müller von Reichenstein, minéralogiste autrichien, a travaillé avec un minerai appelé or allemand. De ce minerai, il a obtenu un matériau qui a défié ses tentatives d'analyse et a été appelé par lui metallum problematicum. En 1798, Martin Heinrich Klaproth a confirmé les observations de Müller et établi la nature élémentaire de la substance. Il a nommé l'élément d'après le «corps céleste» de l'homme Tellus, ou la Terre.
Occurrence et préparation
La demande de tellure ne correspond pas à celle du sélénium. Les deux éléments se retrouvent ensemble dans de nombreux minerais; ils peuvent être isolés en utilisant les procédés décrits en rapport avec le sélénium, en obtenant des solutions contenant des sels à la fois des acides sélénieux et tellureux, H 2 SeO 3 et H 2 TeO 3. Lors du traitement de ces solutions avec de l'acide sulfurique, le dioxyde de tellure, TeO 2, se sépare en raison de sa faible solubilité, tandis que l'acide sélénieux reste dissous. Le dioxyde de tellure peut être converti en tellure élémentaire par traitement avec du dioxyde de soufre; un processus électrolytique est utilisé pour purifier le produit.
Le Japon, les États-Unis et le Canada sont les plus grands producteurs mondiaux de tellure.