Radium (Ra), élément chimique radioactif, le plus lourd des métaux alcalino-terreux du groupe 2 (IIa) du tableau périodique. Le radium est un métal blanc argenté qui ne se produit pas librement dans la nature.
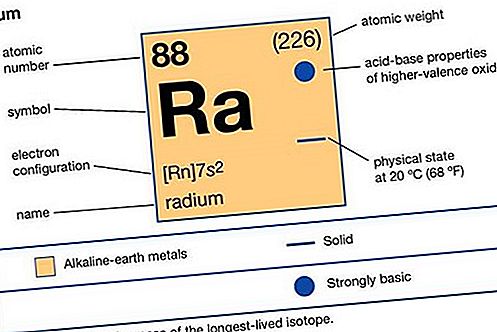

métal alcalino-terreux
baryum (Ba) et radium (Ra).
Propriétés des éléments
| numéro atomique | 88 |
|---|---|
| isotope le plus stable | 226 |
| point de fusion | environ 700 ° C (1300 ° F) |
| point d'ébullition | pas bien établi (environ 1 100 à 1 700 ° C [2 000 à 3 100 ° F]) |
| gravité spécifique | Environ 5 |
| état d'oxydation | +2 |
| configuration électronique | [Rn] 7s 2 |
Occurrence, propriétés et utilisations
Le radium a été découvert (1898) par Pierre Curie, Marie Curie, et un assistant, G.Bémont, après que Marie Curie a observé que la radioactivité de la pitchblende était quatre ou cinq fois supérieure à celle de l'uranium qu'il contenait et n'était pas entièrement expliquée sur la base de polonium radioactif, qu'elle venait de découvrir dans les résidus de pitchblende. La nouvelle substance puissamment radioactive pouvait être concentrée avec du baryum, mais, comme son chlorure était légèrement plus insoluble, il pouvait être précipité par cristallisation fractionnée. La séparation a été suivie par l'augmentation de l'intensité des nouvelles raies dans le spectre ultraviolet et par une augmentation régulière du poids atomique apparent du matériau jusqu'à ce qu'une valeur de 225,2 soit obtenue, remarquablement proche de la valeur actuellement acceptée de 226,03. En 1902, 0,1 gramme de chlorure de radium pur était préparé en raffinant plusieurs tonnes de résidus de pitchblende, et en 1910, Marie Curie et André-Louis Debierne avaient isolé le métal lui-même.
Trente-quatre isotopes du radium, tous radioactifs, sont connus; leur demi-vie, à l'exception du radium-226 (1 600 ans) et du radium-228 (5,75 ans), est inférieure à quelques semaines. Le radium-226 à longue durée de vie se trouve dans la nature en raison de sa formation continue à partir de la désintégration de l'uranium-238. Le radium est donc présent dans tous les minerais d'uranium, mais il est plus largement distribué car il forme des composés hydrosolubles; La surface de la Terre contient environ 1,8 × 10 13 grammes (2 × 10 7 tonnes) de radium.
Étant donné que tous les isotopes du radium sont radioactifs et de courte durée à l'échelle géologique, tout radium primitif aurait disparu depuis longtemps. Par conséquent, le radium se produit naturellement uniquement en tant que produit de désintégration dans les trois séries de désintégration radioactive naturelle (thorium, uranium et actinium). Le radium-226 fait partie de la série de la désintégration de l'uranium. Son parent est le thorium-230 et sa fille le radon-222. Les autres produits de désintégration, anciennement appelés radium A, B, C, C ′, C ″, D, etc., sont les isotopes du polonium, du plomb, du bismuth et du thallium.