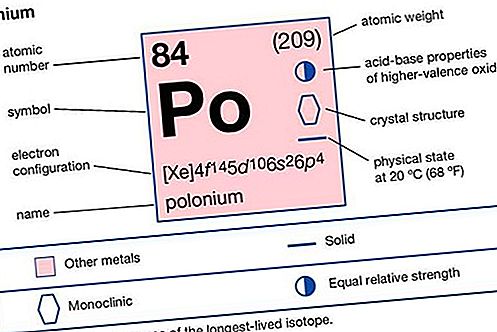
Polonium (Po), un élément métallique radioactif gris argenté ou noir du groupe oxygène (Groupe 16 [VIa] dans le tableau périodique). Premier élément découvert par analyse radiochimique, le polonium a été découvert en 1898 par Pierre et Marie Curie, qui enquêtaient sur la radioactivité d'une certaine pitchblende, un minerai d'uranium. La radioactivité très intense non attribuable à l'uranium a été attribuée à un nouvel élément, nommé par eux d'après la patrie de Marie Curie, la Pologne. La découverte a été annoncée en juillet 1898. Le polonium est extrêmement rare, même dans la pitchblende: 1 000 tonnes de minerai doivent être traitées pour obtenir 40 milligrammes de polonium. Son abondance dans la croûte terrestre est d'environ une partie sur 10 15. Il se produit dans la nature en tant que produit de désintégration radioactif de l'uranium, du thorium et de l'actinium. La demi-vie de ses isotopes varie d'une fraction de seconde à 103 ans; l'isotope naturel le plus courant du polonium, le polonium-210, a une demi-vie de 138,4 jours.
Le polonium est généralement isolé des sous-produits de l'extraction du radium des minéraux d'uranium. Dans l'isolement chimique, le minerai de pitchblende est traité avec de l'acide chlorhydrique et la solution résultante est chauffée avec du sulfure d'hydrogène pour précipiter le monosulfure de polonium, PoS, ainsi que d'autres sulfures métalliques, tels que celui du bismuth, Bi 2 S 3, qui ressemble au monosulfure de polonium étroitement dans le comportement chimique, bien qu'il soit moins soluble. En raison de la différence de solubilité, une précipitation partielle répétée du mélange de sulfures concentre le polonium dans la fraction la plus soluble, tandis que le bismuth s'accumule dans les parties les moins solubles. Cependant, la différence de solubilité est faible et le processus doit être répété plusieurs fois pour obtenir une séparation complète. La purification est réalisée par dépôt électrolytique. Il peut être produit artificiellement en bombardant du bismuth ou du plomb avec des neutrons ou avec des particules chargées accélérées.
Chimiquement, le polonium ressemble aux éléments tellure et bismuth. On connaît deux modifications du polonium, une forme α et une forme β, toutes deux stables à température ambiante et possédant des caractéristiques métalliques. Le fait que sa conductivité électrique diminue à mesure que la température augmente place le polonium parmi les métaux plutôt que les métalloïdes ou les non-métaux.
Parce que le polonium est très radioactif - il se désintègre en un isotope stable du plomb en émettant des rayons alpha, qui sont des flux de particules chargées positivement - il doit être manipulé avec une extrême prudence. Lorsqu'il est contenu dans des substances telles que la feuille d'or, qui empêchent le rayonnement alpha de s'échapper, le polonium est utilisé industriellement pour éliminer l'électricité statique générée par des processus tels que le laminage du papier, la fabrication de feuilles en plastique et le filage de fibres synthétiques. Il est également utilisé sur les brosses pour éliminer la poussière des films photographiques et en physique nucléaire comme source de rayonnement alpha. Des mélanges de polonium avec du béryllium ou d'autres éléments légers sont utilisés comme sources de neutrons.
Propriétés des éléments
| numéro atomique | 84 |
|---|---|
| poids atomique | 210 |
| point de fusion | 254 ° C (489 ° F) |
| point d'ébullition | 962 ° C (1764 ° F) |
| densité | 9,4 g / cm 3 |
| états d'oxydation | −2, +2, +3 (?), +4, +6 |
| configuration électronique. | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 6s 2 6p 4 |







![Un goût de miel film de Richardson [1961] Un goût de miel film de Richardson [1961]](https://images.thetopknowledge.com/img/entertainment-pop-culture/4/taste-honey-film-richardson-1961.jpg)




![Seconde bataille d'Ypres Première Guerre mondiale [1915] Seconde bataille d'Ypres Première Guerre mondiale [1915]](https://images.thetopknowledge.com/img/world-history/4/second-battle-ypres-world-war-i-1915.jpg)
