Thorium (Th), élément chimique radioactif de la série des actinoïdes du tableau périodique, numéro atomique 90; c'est un combustible de réacteur nucléaire utile. Le thorium a été découvert (1828) par le chimiste suédois Jöns Jacob Berzelius. Il est blanc argenté mais devient gris ou noir lorsqu'il est exposé à l'air. Il est environ deux fois plus abondant que le plomb et est trois fois plus abondant que l'uranium dans la croûte terrestre. Le thorium est récupéré commercialement à partir de la monazite minérale et se trouve également dans d'autres minéraux tels que la thorite et la thorianite. Le thorium métal a été produit en quantités commerciales par réduction du tétrafluorure (ThF 4) et du dioxyde (ThO 2) et par électrolyse du tétrachlorure (ThCl 4). L'élément a été nommé pour le dieu nordique Thor.

élément actinoïde: applications pratiques des actinoïdes
Le thorium a également une grande valeur économique, car l'un de ses isotopes, le thorium-232, peut être converti en
Le métal peut être extrudé, laminé, forgé, embouti et filé, mais l'étirage est difficile en raison de la faible résistance à la traction du thorium. Ces propriétés physiques et d'autres telles que les points de fusion et d'ébullition sont fortement affectées par de petites quantités de certaines impuretés, telles que le dioxyde de carbone et de thorium. Le thorium est ajouté au magnésium et aux alliages de magnésium pour améliorer leur résistance à haute température. Il a été utilisé dans des cellules photoélectriques commerciales pour mesurer la lumière ultraviolette de longueurs d'onde allant de 2000 à 3750 angströms. Ajouté au verre, le thorium donne des verres à indice de réfraction élevé, utiles pour les applications optiques spécialisées. Il était autrefois très demandé en tant que composant de manchons pour lampes à gaz et à pétrole et a été utilisé dans la fabrication de filaments de tungstène pour ampoules et tubes à vide.
La radioactivité du thorium a été découverte indépendamment (1898) par le chimiste allemand Gerhard Carl Schmidt et par la physicienne française Marie Curie. Le thorium naturel est un mélange d'isotopes radioactifs, principalement le thorium-232 à très longue durée de vie (demi-vie de 1,40 × 10 10 ans), le parent de la série de désintégration radioactive du thorium. D'autres isotopes se produisent naturellement dans les séries de désintégration de l'uranium et de l'actinium, et le thorium est présent dans tous les minerais d'uranium. Le thorium-232 est utile dans les réacteurs surgénérateurs parce qu'en capturant les neutrons lents, il se désintègre en uranium-233 fissile. Des isotopes synthétiques ont été préparés; le thorium-229 (demi-vie de 7880 ans), formé dans la chaîne de désintégration originaire de l'élément actinoïde synthétique neptunium, sert de traceur au thorium ordinaire (thorium-232).
Le thorium présente un état d'oxydation de +4 dans presque tous ses composés. L' ion Th 4+ forme de nombreux ions complexes. Le dioxyde (ThO 2), une substance très réfractaire, a de nombreuses applications industrielles; le nitrate de thorium est disponible sous forme de sel commercial.
Propriétés des éléments
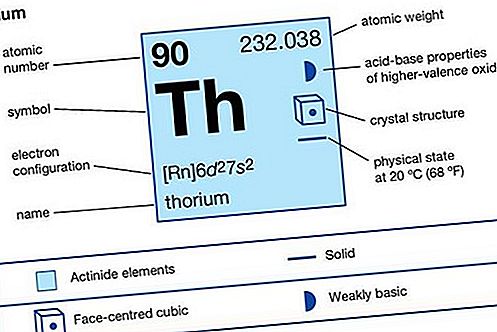
| numéro atomique | 90 |
|---|---|
| poids atomique | 232.038 |
| point de fusion | environ 1700 ° C (3100 ° F) |
| point d'ébullition | environ 4000 ° C (7200 ° F) |
| gravité spécifique | environ 11,66 (17 ° C) |
| état d'oxydation | +4 |
| configuration électronique de l'état atomique gazeux | [Rn] 6d 2 7s 2 |













