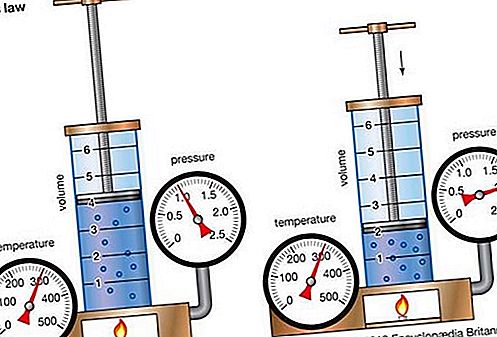
Loi de Boyle, également appelée loi de Mariotte, une relation concernant la compression et l'expansion d'un gaz à température constante. Cette relation empirique, formulée par le physicien Robert Boyle en 1662, affirme que la pression (p) d'une quantité donnée de gaz varie inversement avec son volume (v) à température constante; c'est-à-dire, sous forme d'équation, pv = k, une constante. La relation a également été découverte par le physicien français Edme Mariotte (1676).
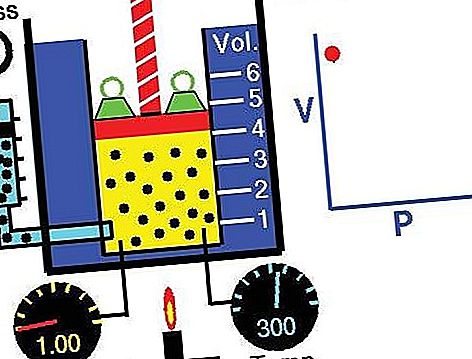
La loi peut être dérivée de la théorie cinétique des gaz en supposant un gaz parfait (idéal) (voir gaz parfait). Les gaz réels obéissent à la loi de Boyle à des pressions suffisamment basses, bien que le produit pv diminue généralement légèrement à des pressions plus élevées, où le gaz commence à s'écarter du comportement idéal.