Loi de proportions définies, affirmant que chaque composé chimique contient des proportions fixes et constantes (en masse) de ses éléments constitutifs. Bien que de nombreux expérimentateurs aient longtemps supposé la vérité du principe en général, le chimiste français Joseph-Louis Proust a d'abord accumulé des preuves concluantes à son sujet dans une série de recherches sur la composition de nombreuses substances, en particulier les oxydes de fer (1797). Un autre chimiste français, Claude Berthollet, qui détenait des proportions indéfinies, contesta les conclusions de Proust, mais le chimiste écossais Thomas Thomson confirma certaines d'entre elles et écrivit dans son article «Chimie» dans le Supplément à l'Encyclopædia (1801) que Proust avait définitivement prouvé « les métaux ne sont pas capables de degrés d'oxydation indéfinis. » Le principe a ensuite été concrètement formulé par le chimiste anglais John Dalton dans sa théorie atomique chimique (1808).
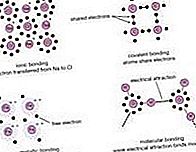
liaison chimique: la loi des proportions définies
L'expérimentation de Lavoisier a inspiré de nouvelles études qui ont finalement abouti à un renversement de l'idée que la matière est une structure